Dieta mamy karmiącej piersią – aktualizacja 2018
#KarmieJemWszystko
Dieta mamy karmiącej to MIT, spadek po poprzednim systemie, następstwo braku wiedzy na temat laktacji, nie istnieje coś takiego. Mama karmiąca powinna się po prostu zdrowo odżywiać, stosować zróżnicowana dietę, bez suplementów w kolorowych pigułkach. Tak, możesz jeść wszystko, chociaż nie zaleca się fastfoodów i alkoholu (o tym niżej), dieta powinna być podobna do tej z okresu ciąży, bogata w warzywa, owoce i nieprzetworzone produkty, powinna być zgodna z nową piramidą żywieniową.
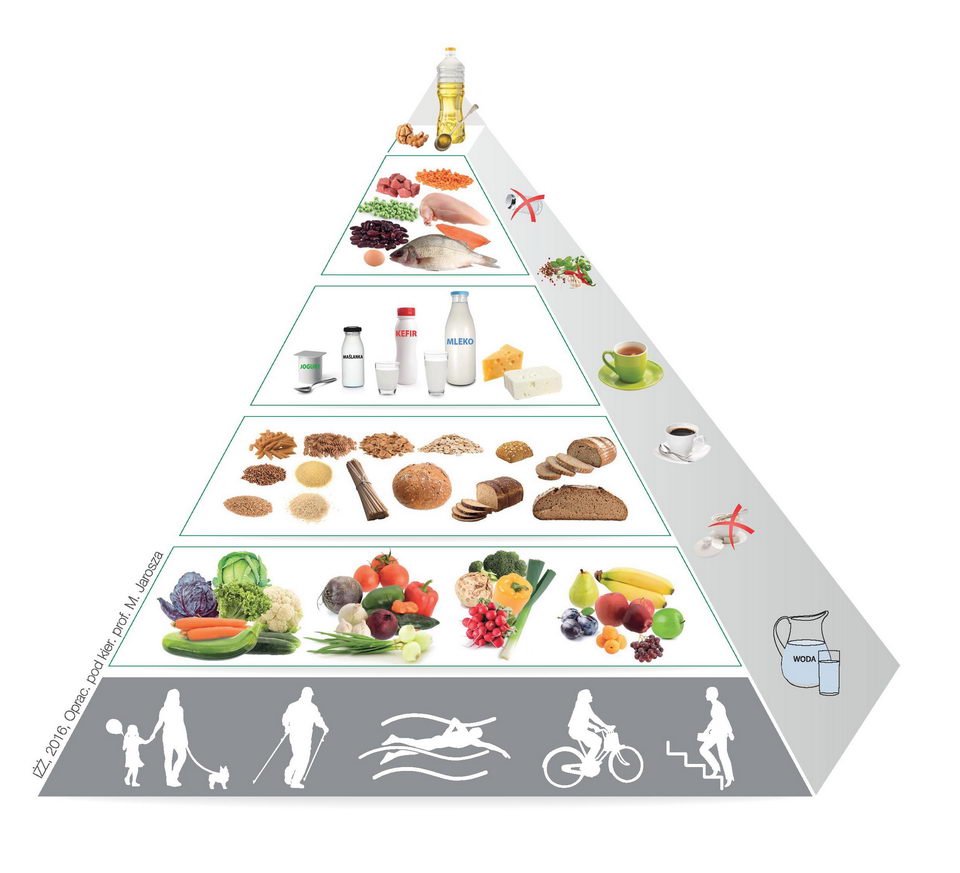
Skąd się bierze pokarm?
Z ust wstępnie rozdrobniony i nadtrawiony enzymami zawartymi w ślinie pokarm trafia do żołądka. Czas trawienia w żołądku zależy od tego co mama je, ale także co jadła bezpośrednio przedtem bo dajmy na to dziecko zareagowało na gotowaną marchewkę – sama marchewka gotowana nie należy do potraw ciężkostrawnych, ale jeśli pojawiła się w towarzystwie mięsa, które w żołądku zalega 6-8 godzin!!! to wiadomo, że reakcja nastąpi odpowiednio później. Kiedy już pokarm strawiony w żołądku, go opuści, przenosi się do dwunastnicy gdzie przechodzi kolejny etap trawienia, a następnie dalej do jelita cienkiego, gdzie następuje powolny proces przesuwania treści jelitowej dalej dzięki tzw ruchom robaczkowym, dzięki wyrostkom – kosmkom dochodzi to wchłaniania substancji odżywczych do krwi: proteiny, minerały, witaminy, tłuszcze, cukry proste, ale także leki, toksyny, konserwanty itd. Krew prowadzi wszystko do wątroby, pełniącej w naszym organizmie funkcje filtra ona wszystko metabolizuje i przerabia na łatwe do przyswojenia substancje, po opuszczeniu wątroby krew rusza w dalszą drogę do komórek organizmu oraz do gruczołów mlecznych, które pobierają z krwi wszelkie niezbędne substancje: przeciwciała, witaminy, minerały, składniki odżywcze, niestety nie wszystko zostało zatrzymane w wątrobie i niestety nie wszystko zostaje odfiltrowane w procesie przetwarzania krwi na mleko. Potencjalnie alergizujące białka, niektóre toksyny, wirusy, konserwanty i leki przechodzą przez te bariery i dostają się do mleka, u bardziej wrażliwych niemowląt moze sie to objawiać kolka, wypryskiem alergicznym, czy gorszym stolcem. Jednak nawet takie objawy nie są wskazaniem do stosowania diet eliminacyjnych w świetle badań z ostatnich 2 lat. jedynym bezwzględnym wskazaniem do stosowania ścisłej diety eliminacyjnej jest potwierdzona anafilaksja na dane białko, ale nie na to białko i wszystkie okoliczne, np, jeśli stwierdzono reakcję na beta-laktoglobulinę, to eliminujemy mleko i produkty mlekopochodne, a nie przy okazji wołowinę, a na wszelki wypadek wieprzowinę, jeśli na białko kurze, to eliminujemy białko, ale nie żółtko i kurczaka (a tym bardziej nie cały drób).
Co ważne, jeśli mama decyduje sie wyeliminować jakiś składnik to jedyne jakie należy rozważyć to białko mleka krowiego, ewentualnie jajo i na okres nie dłuższy niż 3 max 6 tyg. Matka dietę powinna z powrotem rozszerzyć najpóźniej w 6-stym miesiącu życia dziecka, aby w 7, zgodnie ze schematem rozszerzania diety, można było wprowadzić do diety dziecka produkty uzupełniające w tym białka mlek czy jajo. Alergolodzy podkreślają wagę nie przeciągania diety eliminacyjnej dłużej niż 3 miesięcy w skrajnych przepadkach.
Więcej nt diety eliminacyjnej przeczytacie w artykułach:
- Dieta mamy alergika i dieta eliminacyjna – aktualizacja 2017,
- Dieta eliminacyjna – raz jeszcze,
- Dlaczego mleko mamy nie powoduje alergii?
- Postępowanie w przypadku alergii u dziecka – najnowsze zalecenia Towarzystw Alergologicznych oraz konsultantów laktacyjnych
W wielu publikacjach udowodniono ochronną role diety śródziemnomorskiej w ograniczeniu reakcji alergicznych
Tak więc mama odżywia się zdrowo, dostarczając z pokarmu wszystkich niezbędnych składników: witamin, minerałów, oraz składników odżywczych. Cały czas powinna obserwować dziecko. Jeśli niepokoi ją zachowanie dziecka: jest niespokojnie, płacze, podkurcza przy tym nóżki, może zauważyć czy ma to związek z konkretnym produktem, podobnie w przypadku ewentualnej wysypki, lub nieprawidłowego stolca dziecka (ciemnozielonym, o nieprzyjemnym, intensywnie kwaśnym zapachu, mogą pojawić się pasma śluzu, krew lub/i stolec może być pienisty) wówczas jest wskazówką ze coś dziecku szkodzi, taki składnik należy wykluczyć z diety mamy karmiącej na pewien czas, np na miesiąc. Jednak nie od urodzenia na wszelki wypadek, tylko wówczas kiedy widzimy, że wyraźnie szkodzi. Pamiętajmy, że pokarm jest niezależny od diety mamy, ale to czego mama nie dostarczy z pokarmem dziecko zabierze z organizmu mamy, dlatego zróżnicowana dieta jest niezwykle ważna dla zdrowia i samopoczucia mamy.
Czyli co tak konkretnie może jeść mama karmiąca piersią??
Karmienie piersią nie wyklucza normalnej diety. Można jeść wszystko (w granicach zdrowego rozsądku):
- orzechy i pestki (dynia, słonecznik)
- miód,
- mięso i ryby także surowe (a wiec tatar i sushi także),
- sery i szynki dojrzewające,
- sery pleśniowe,
- owoce małostkowe (jabłka, gruszki)
- dużopestkowe (śliwki, czereśnie, wiśnie, nektarynki )
- drobnopestkowe (jagody, borówki, truskawki),
- można smażona cebulkę,
- kapuchę,
- fasolkę,
- kiełki,
- kiszonki,
- grzyby leśne, mun, boczniaki i pieczarki,
- można jeść czekoladę
- cytrusy
- i nawet można to wszystko popić gazowana wodą.


Mleko robi się z krwi, a nie z treści jelitowej.
Mama powinna się dobrze odżywiać, mieć zdrową i zróżnicowaną dietę.
- ryby, zwłaszcza surowe – są bardzo zdrowe, polecam rodzimego śledzia, a także szprotki i makrele wędzone na zimno – są świetnym źródłem kwasów Omega 3 (które są wrażliwe na obróbkę termiczną)
- owoce i warzywa – dostarczają witamin
- mięso – białka
- orzechy i nabiał – wapń
- cytrusy – wit C
- kiszonki – maja właściwości probiotyczne
- kasze – dostarczają minerałów
- pestki dyni, słonecznika, tłuszczy nienasyconych (są lepsze niż oleje, gdyż dostarczają błonnika więcej, nt olei można przeczytać tutaj)
A wiec mamy jedzcie na zdrowie co chcecie.
Obserwować dziecko. A dietę eliminacyjną wprowadza się W OSTATECZNOŚCI ze wskazań medycznych, a nie na wszelki wypadek.

PŁYNY
Mama karmiąca piersią powinna się nawadniać, źródła podają różnie od 1,5-3 litrów na dobę, jednak nie oznacza to, że mama ma się zmuszać do picia, należy pamiętać że oprócz wody, płyny można pozyskać pijąc herbaty ziołowe i owocowe, soki (najlepiej świeżowyciskane, ewentualnie 1-dniowe, jeśli pasteryzowane, to najlepiej w szklanych butelkach, mleko i przetwory, zupy, czy jedząc owoce i warzywa.
Można pic kawę (do 4 filiżanek dziennie), ale prawdziwą, najlepiej parzoną w ekspresie ciśnieniowym lub kafeterze, ze względu na fakt, że rozpuszczalna jest produktem wysokoprzetworzonym i nie ma żadnych wartości ani aromatycznych, nie zawiera olejków eterycznych, ani smakowych, ani odżywczych i nie powinna się znaleźć w diecie mamy karmiącej piersią. Mitem jest, że kawa wypłukuje magnez z organizmu. Świeżo zmielona i zaparzona kawa, korzystnie wpływa na organizm człowieka.
polecam też artykuły okolicznościowe: Co może w Święta jeść mama karmiąca piersią i Wielkanocna uczta
Źródła:
- http://kellymom.com/
- http://www.aap.org/en-us/Pages/Default.aspx
- http://www.who.int/nutrition/en/
- http://www.kobiety.med.pl/cnol/
- http://milkpower.pl/dieta-mamy-alergika/
- Greaves M. A causal mechanism for childhood acute lymphoblastic leukaemia, Nature Reviews Cancer (2018)
- Rudant, J. et al. Childhood acute leukemia, early common infections, and allergy: the ESCALE Study. Am. J. Epidemiol. 172, 1015–1027 (2010)
- Chatzi L., , „Mediterranean diet in pregnancy is protective for wheeze and atopy in childhood„,
- . De Batlle, J. Garcia-Aymerich, A. Barraza-Villarreal i wsp „Mediterranean diet is associated with reduced asthma and rhinitis in Mexican children„, Allergy. 2008 Oct;63(10):1310-6.
- G. HATTEVIG, B. KJELLMAN, N. SIGURS, i wsp „Effect of maternal avoidance of eggs, cow’s milk and fish during lactation upon allergic manifestations in infants„, Clin Exp Allergy. 1989 Jan;19(1):27-32.
- Kirsi M. Järvinen, M.D., Ph.D., Jennifer E. Westfall, Ph.D., Max S. Seppo, i wspólnicy, Role of maternal elimination diets and human milk IgA in development of cow’s milk allergy in the infants, Clinical &
- Experimental Allergy, Volume 44, Issue 1, pages 69–78, January 2014
Niniejszy tekst ma charakter informacyjny i nie zastąpi indywidualnej konsultacji z lekarzem pediatrą, specjalistą, dietetykiem i doradcą laktacyjnym, decyzję o podjęciu dalszych kroków mama musi podjąć sama na podstawie uzyskanej wiedzy.






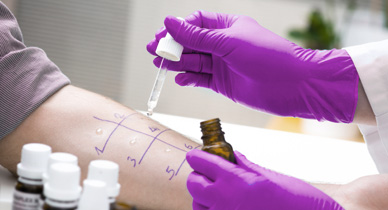




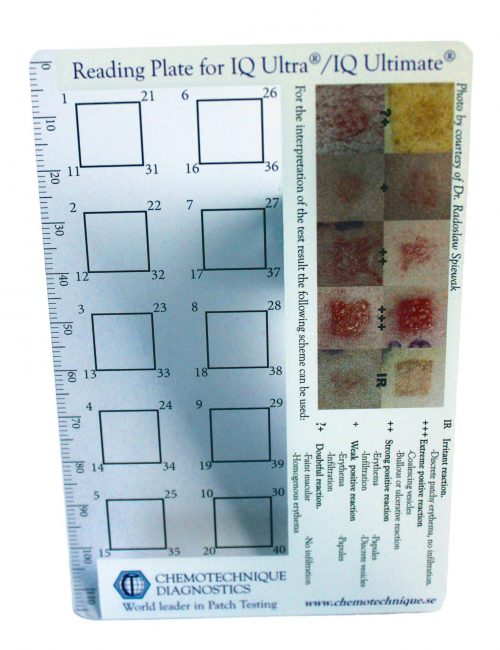
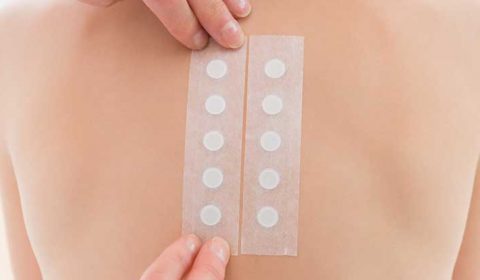 Ostatnia odmiana testów. Polega na umieszczeniu w specjalnym „naparstku” żelu z alergenem. Wszystkie „naparstki” umieszcza się na plastrze a następnie przykleja cały pasek na skórę pleców. Alergeny oznaczane w tym teście to głównie: metal, składniki kosmetyków, antybiotyki.
Ostatnia odmiana testów. Polega na umieszczeniu w specjalnym „naparstku” żelu z alergenem. Wszystkie „naparstki” umieszcza się na plastrze a następnie przykleja cały pasek na skórę pleców. Alergeny oznaczane w tym teście to głównie: metal, składniki kosmetyków, antybiotyki.