SARS-CoV-2 / COVID-19 – ciąża, poród, karmienie piersią
KORONAWIRUSY
To wirusy typu RNA, których nazwa pochodzi od przypominających koronę słoneczną wypustek wirionu. Większość z nich powoduje infekcje jedynie u zwierząt, ale istnieje grupa wirusów, która wywołuje powszechne infekcje u ludzi. Ludzkie koronawirusy – „HCoV” są przyczyną wirusowego zapalenia płuc i oskrzeli. Szerzą się drogą kropelkową, czyli poprzez wydzielinę z dróg oddechowych (kaszel, kichanie) i kontakt z zakażonymi powierzchniami. Infekcje koronawirusowe pojawiają się głównie wiosną i stanowią 30% wszystkich infekcji grypopodobnych w sezonie.
-

Mikrobiologia lekarska. Red. Heczko, Piotr B.; Pietrzyk, Agata; Wróblewska, Marta. Warszawa: PZWL Wydawnictwo Lekarskie, 2014 , s. 337
Ludzkie koronawirusy w przeważającej większości atakują górne drogi oddechowe, często bezobjawowo. Znacznie rzadziej zajmują drogi dolne, a o ciężkim przebiegu choroby mówimy głównie w kontekście niemowląt, osób starszych i tych z upośledzoną odpornością. Infekcje wirusowe tego typu mogą zaostrzać astmę oskrzelową.
Niestety, tak jak i w przypadku większości chorób wirusowych, tak i w przebiegu infekcji koronawirusowych brak specyficznego leczenia. Stosuje się jedynie leczenie objawowe.
SARS-CoV – Wirus ciężkiego ostrego zespołu oddechowego (serve accute respiratory syndrome)
Pod koniec 2002 roku w Chinach pojawił się SARS-CoV. Przez lata ten ODZWIERZĘCY wirus atakował głównie cywety i jenoty, a do człowieka dotarł prawdopodobnie za pośrednictwem nietoperzy podkowiastych. Rozprzestrzeniał się drogą kropelkową, a okres jego wylęgania wynosił 2-3 dni (max. 10).
Do głównych objawów SARS – CoV należały:
– gorączka powyżej 38
– ból gardła
– osłabienie
– suchy kaszel
– biegunka
– narastająca duszność i niewydolność oddechowa => atypowe zapalenie płuc
Wirus powodował uszkodzenie pęcherzyków płucnych oraz poliferację, czyli nadmierne rozmnażanie komórek nabłonkowych i wzrost liczby makrofagów (układ odpornościowy).
Ostatecznie wirus SARS – CoV dotarł do 32 krajów, w których zachorowało 8098 osób, a zmarło 774. Współczynnik śmiertelności plasował się na poziomie 10%.
MERS-CoV – ciężkie zapalenie płuc Bliskiego Wschodu (Middle East respiratory syndrome)
Kolejny 'zabójczy’ wirus z grupy koronawirusów – MERS-CoV pojawił się w 2012 roku w krajach Bliskiego Wschodu i szybko rozprzestrzenił na Europę, USA i Azję.
Do końca stycznia 2020 roku potwierdzono dodatnim testem labolatoryjnym 2 519 przypadków MERS. 866 osób zmarło. Współczynnik śmiertelności sięgnął 30-40%, a wśród zmarłych znalazła się szeroka grupa pracowników medycznych – 20% wszystkich przypadków śmiertelnych.
2121 przypadków odnotowano w Arabii Saudyjskiej, w tym 788 zgonów, co daje współczynnik śmiertelności 37,1%, ponadto choroba rozprzestrzeniła się w innych krajach bliskiego wschodu takich jak Zjednoczone Emiraty Arabskie, Jemen, Oman, Katar, Kuwejt, Iran i Liban czyli kraje, w których tradycyjnie korzysta sie z transportu karawan dromaderów. Kolejne przypadki zachorowań i śmiertelne pojawiają się co roku, dotyczą głównie mężczyzn w wieku 50-59 lat w pierwszej infekcji w połączeniu ze śmiertelnością, w grupie 30-39 częściej pojawia sie ponowna infekcja, zaś w grupie 70-79 jest najwyższy odsetek śmiertelności w następstwie ponownej infekcji.
Choroba dotarła ostatecznie do 27 krajów.
Wirusem tym człowiek zaraził się od dromaderów, ale pierwszym ogniwem w łańcuchu zachorowań były najprawdopodobniej nietoperze, a wielbłądy jedynie pośredniczyły w procesie.
2019-nCoV / SARS-CoV-2 / COVID-19
Początkowo nowy koronawirus miał nazwę nCov-2019
n – new
CoV – CoronaVirus – koronawirus (skrót odnoszący sie do wszystkich koronawirusów)
2019 – po raz pierwszy zaobserwowany w Wuhan w prowincji Hubei w Chinach w 2019 roku
SARS-CoV-2 – ze względu na podobieństwo do wirusa SARS-CoV z 2002 roku nadano mu taką samą nazwę ale dodano cyfrę 2 dla rozróżnienia, powoduje podobne objawy ciężkiego ostrego zespołu oddechowego (SARS-serve accute respiratory syndrome)
COVID-19 – to skrót od coronavirus disease czyli choroba koronawirusowa roku 2019
W połowie grudnia 2019 roku w chińskiej prowincji Hubei pojawiły się pierwsze zachorowania na COVID-19. Niestety, podobnie jak w przypadku SARS, władze chińskie zataiły przed WHO i opinią publiczną informacje o nowym koronawirusie. Tymczasem do 25 stycznia odnotowano 1320 potwierdzonych przypadków, z czego 237 zarażonych znalazło się w stanie ciężkim, a 41 osób zmarło. W większości pierwsi zarażeni mieli kontakt z lokalnym rynkiem zwierząt i owoców morza.
Analiza genomu wykazała różnicie pomiędzy nowym wirusem, a jego poprzednikami – SARS-CoV i MERS-CoV, jednakże cała trójka należy do wspólnej grupy betakoronawirusów. Pomimo wielu teorii spiskowych ustalono, że wirus z Wuhan nie był w żaden sposób rekombinowany i jest zgodny z BatCoV RaTG13 wykrytym u nietoperzy z prowincji Yunnan.
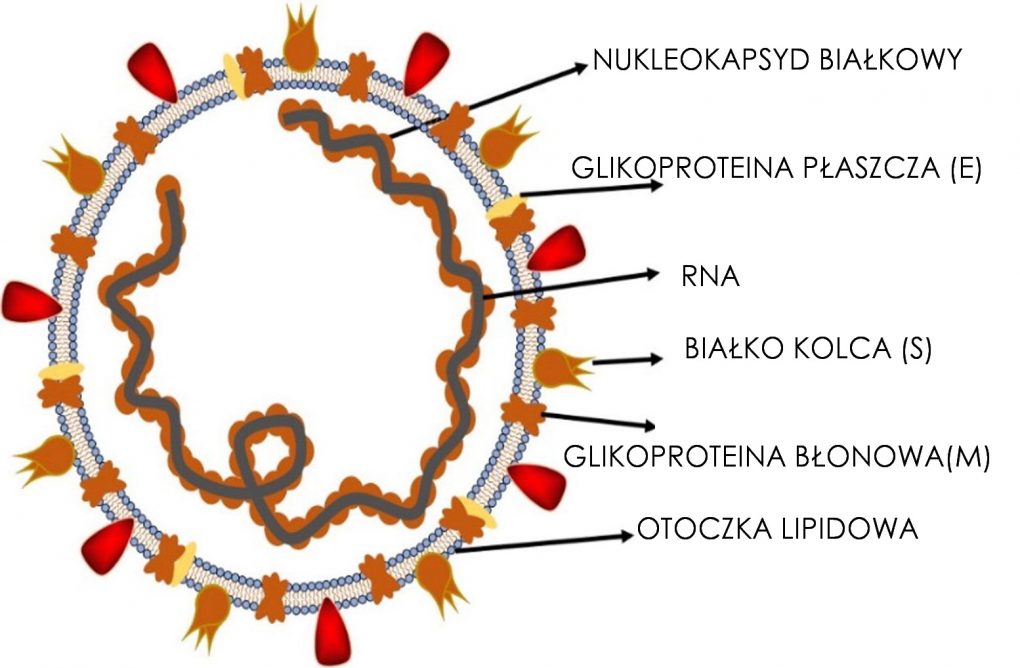
COVID-19 infection: origin, transmission, and characteristics of human coronaviruses
Author links open overlay panelMuhammadAdnan Shereenab1SulimanKhana1
AbeerKazmicNadiaBashiraRabeeaSiddiquea
Kolejne badanie nad wirusem podaje, że SARS-CoV-2 może wiązać ludzkie ACE2 z dużym powinowactwem, jednak reakcja nie jest idealnie zgodna, co jest wynikiem naturalnej selekcji na ludzkim ACE2, co stanowi silny dowód na to, że wywołujący COVID-19 wirus SARS-CoV-2 nie jest produktem manipulacji człowieka.

COVID-19 infection: origin, transmission, and characteristics of human coronaviruses
Author links open overlay panelMuhammadAdnan Shereenab1SulimanKhana1
AbeerKazmicNadiaBashiraRabeeaSiddiquea
JAK DZIAŁ SARS-COV-2?
DROGI INWAZJI
Do zarażenia dochodzi drogą kropelkową, czyli poprzez kontakt z wydzielinami z dróg oddechowych: kasłanie, kichanie, oddychanie oraz poprzez kontakt powierzchnią, na której znajdują się wyżej wymienione wydzieliny. Badanie opublikowane 14 marca wykazało, że wirus jest w stanie przetrwać 4 godziny na powierzchni miedzianej, 24 na papierowej/tekturowej oraz aż 2-3 dni na powierzchni z tworzywa sztucznego lub stali nierdzewnej.
W ramach testów rozpylono także SUCHEGO wirusa, a taki gaz utrzymał się w powietrzu przez 6 godzin. Choć to ciekawa informacja, to eksperymentu nie można przenosić jeden do jednego na warunki życiowe. Wirus wydostający się z dróg oddechowych jest obciążony cząsteczkami ludzkiej wydzieliny i w związku ze swoją wagą opada na powierzchnie, na które natrafi. AKTUALNIE UZNAJE SIĘ, ŻE W POWIETRZU UTRZYMUJE SIĘ OK 3 GODZIN.
ZARAŹLIWOŚĆ
Do zarażenia COVID-19 dochodzi podczas:
- rozmowy twarzą w twarz przez dłużej niż 15 minut w odległości do 2 metrów
- przebywania w jednym pomieszczeniu z zakażonym przez co najmniej 2h
- dotykania ręką skażonej powierzchni, a następnie okolicy twarzy
PROFILAKTYKA
- Jeśli musisz jechać autobusem wsiądź później i wysiądź wcześniej, przejdź piechota ile się da, aby skrócić ewentualny czas ekspozycji do minimum.
- W kolejce zachowaj odstęp 1-2 m pomiędzy kolejnymi osobami.
- Kupuj przez internet, nie wychodź z domu jeśli nie musisz.
- Myj ręce, wirus rozpada się pod wpływem mydła.
- Nie dotykaj klamek, uchwytów – do otwierania drzwi używaj łokcia, biodra lub wchodź „z kopa”.
- Jeśli musisz dotknąć klamki, uchwytu, poręczy zrób to
przez ręcznik papierowy / chusteczkę lub w rękawiczkach, a następnie zdezynfekuj je lub umyj tak, jak myjesz ręce. - Maseczki na twarzy nie chronią przed infekcja, ale ograniczają dotykanie twarzy (rękawiczki jednorazowe również), ograniczają też rozprzestrzenianie się infekcji od bezobjawowych nosicieli.
OBJAWY I OKRES INKUBACJI
Od zarażenia do pojawienia się pierwszych objawów COVID-19 mija od 2 do 14 dni – przeciętnie 3 do 5. Należy jednak mieć na uwadze, że w pojedynczych przypadkach zaobserwowano czas dłuższy 21, a nawet 27 dni. Obecnie za taki stan rzeczy podejrzewa się ponowną ekspozycję na działanie wirusa w okresie 14 dni poprzedzających wystąpienie pierwszych objawów.
Nie należy zapominać, że symptomy zakażenia mogą wcale się nie pojawić, a bezobjawowy nosiciel również jest zagrożeniem dla innych. Takie przypadki były obserwowane w Korei (o czym później przy okazji diagnostyki).
Do głównych objawów COVID-19 należą:
- suchy kaszel
- wysoka temperatura powyżej 38 stC
- uczycie zmęczenia
- bóle mięśni
- bóle głowy
- ból gardła
- duszności
- trudności z oddychaniem
- biegunka
- katar, zatkany nos
- zapalenie spojówek
19 marca w American Jurnal of Gastroenterology zostały oblicowane badania, które donoszą, że połowa pacjentów w prowincji Hubei zgłosiła się do szpitala z powodu problemów z układem pokarmowych, a nie z układem oddechowym. Należały do nich głównie biegunka ~30% oraz wymioty i ból brzucha. Ponadto duża grupa pacjentów cierpiała na anoreksję (~84%). Rzuca to nowe światło na rozpoznanie choroby koronawirusowej i jej symptomów, gdyż do tej pory zaburzeń pracy układu trawiennego nie brano jej pod uwagę jako głównego symptomu choroby, a traktowano jedynie jako następstwo podawania leków.
DIAGNOSTYKA
Model koreański, singapurki, japoński i hongkoński wykazały, że
najefektywniejszą formą diagnostyki są szerokodostępne testy przesiewowe. W momencie szybkiego przyrostu nowych zachorowań w wymienionych krajach podjęto decyzję o umożliwieniu wykonania testu każdemu z obywateli. Na ternie państwa rozlokowano tzw. punkty uliczne, gdzie można wykonać szybkie testy kasetkowe – zbliżone do testów ciążowych.
Badania przesiewowe prowadzone na ogromną skalę w Korei Pd wykazały, że za rozprzestrzenianie się wirusa w dużej mierze odpowiadają bezobjawowi młodzi ludzie w wieku 20-30 lat. To właśnie w tej grupie wiekowej w wyniku szybkich kasetkowych testów ulicznych wyizolowano najwięcej przypadków zarażenia SARS-CoV-2. Dzięki kwarantannie osób u których nie pojawiły się żadne objawy choroby, bardzo szybko opanowano rozprzestrzenianie się wirusa w społeczeństwie.

Kolejną grupą bezobjawowych nosicieli są dzieci. COVID-19 rozwija się tylko u 0,2% z nich i ma zwykle łagodny przebieg. Jak dotąd prasa doniosła jedynie o jednym śmiertelnym przypadku wśród najmłodszych – trzyletnim dziecku z Iranu, które było obciążone ciężką chorobą współistniejącą – białaczką. W związku z chorobą podstawową dziecko to nie jest brane pod uwagę w statystykach. Pocieszającym jest fakt, że większość zarażonych dzieci jest w stanie dobrym i bez powikłań wraca do pełnego zdrowia.
STATYSTYKI
ŚMIERTELNOŚĆ (16.04.2020), ŹRÓDŁO: OKO.PRESS
Odsetek ofiar śmiertelnych wśród wszystkich wykrytych w Polsce przypadków – 3,8 proc. jest znacznie niższy niż ten sam wskaźnik dla danych globalnych: wśród wszystkich zakażonych do tej pory na świecie 2 mln 53 tys. ludzi zmarło 133 tys., czyli 6,5 proc.
Szczególnie dramatyczny odsetek zgonów wśród wykrytych zakażonych występuje w krajach zachodniej i południowej Europy, które pierwsze zostały zaatakowane przez epidemię:
- we Włoszech – 13,1 proc.;
- w Wielkiej Brytanii – 13,1 proc.;
- w Belgii – 13,0 proc.;
- we Francji 11, 6 proc.;
- w Holandii 11,0 proc.;
- w Hiszpanii 10,5 proc.;
- w Szwecji 10,1 proc.
ŚMIERTELNOŚĆ W ZALEŻNOŚCI OD WIEKU
|
WIEK |
WSPÓŁCZYNNIK ŚMIERTELNOŚCI |
|
80+ lat |
14,8% |
|
70–79 lat |
8,0% |
|
60-69 lat |
3,6% |
|
50–59 lat |
1,3% |
|
40-49 lat |
0,4% |
|
30–39 lat |
0,2% |
|
20–29 lat |
0,2% |
|
10–19 lat |
0,2% |
|
0-9 lat |
BRAK |
ŚMIERTELNOŚĆ W ZALEŻNOŚĆ OD PŁCI
|
PŁEĆ |
ŚMIERTELNOŚĆ
|
|
MĘŻCZYŹNI |
4,7% |
|
KOBIETY |
2,8% |
ŚMIERTELNOŚĆ W ZALEŻNOŚCI OD CHORÓB WSPÓŁISTNIEJĄCYCH
|
CHOROBY WSPÓŁISTNIEJĄCE |
ZDJĘCIA ŚMIERCI |
OCENA ŚMIERCI we |
|
Choroby układu krążenia |
13,2% |
10,5% |
|
Cukrzyca |
9,2% |
7,3% |
|
Przewlekła choroba układu oddechowego (astma oskrzelowa, POChP) |
8,0% |
6,3% |
|
Nadciśnienie |
8,4% |
6,0% |
|
Nowotwór |
7,6% |
5,6% |
|
Bez obciążeń |
0,9% |
CIĄŻA
Większość zarażonych ciężarnych kobiet przejawia skąpe objawy grypopodobne lub objawy charakterystyczne dla przeziębienia. Charakterystyczne dla COVID-19 objawy jak gorączka, kaszel oraz trudności z oddychaniem pojawiają się w ograniczonym zakresie. Cięższe przypadki – zapalenie płuc, niedotlenienie dotyczą głównie osób starszych, przyjmujących leki immunosupresyjne i w przypadku chorób współistniejących: m.in.: cukrzyca, nowotwory czy przewlekłe choroby płuc.
Jak do tej pory nie zanotowano żadnego przypadku przyjęcia kobiety w 34 tygodniu ciąży z koniecznością wykonania cięcia cesarskiego w trybie pilnym ze względu na zagrażającą zamartwicę.
Brak aktualnie danych o wpływie COVID-19 na możliwość poronienia. Nie zaobserwowano także żadnego przypadku wewnątrzmacicznej infekcji płodu oraz wpływu wirusa na rozwój wad wrodzonych.
U przyszłych mam z COVID-19 odnotowano pojedyncze przypadki porodów przedwczesnych, ale nie wykluczono związku z błędami jatrogennymi – ludzkimi. Trudno jednoznacznie stwierdzić przyczynę porodu przedwczesnego oraz oszacować czy faktycznie wcześniejsze rozwiązanie miało związek z infekcją SARS-CoV-2.
ZALECENIA DLA KOBIET W CIĄŻY
Ciężarne powinny odbywać regularne wizyty kontrolne, zgłaszać się na nie bez osoby towarzyszącej, nie wcześniej niż 15 minut przed wyznaczoną godziną. Część wizyt może odbywać się w formie teleporad. Osoby pozostające w domu z kobietami ciężarnymi w miarę swoich możliwości powinny także ograniczyć kontakt z osobami trzecimi.
W celu maksymalnego ograniczenia możliwości styczności z patogenem zaleca się dokonywanie wszelkich zakupów przy pomocy osób z poza gospodarstwa domowego lub za pośrednictwem internetu. Oprócz unikania skupisk ludzkich i wizyt w placówkach handlowych konieczne jest utrzymanie ścisłego reżimu higienicznego.
Kobiety ciężarne nie powinny rezygnować ze spacerów na świeżym powietrzu, jednak z zachowaniem maksymalnej ostrożności, z dala od skupisk ludzkich.
PORÓD KOBIETY BEZ ZAGROŻENIA SARS-COV-2
W związku z wprowadzonym w dniu 20.03.2020 stanem epidemii na terenie Rzeczypospolitej wszystkie porody odbywają się bez udziału osób towarzyszących (rodzina, partner, doula), a jedynie w towarzystwie położnej i lekarza oddziału w którym odbywa się poród.
Jednakże istnieje możliwość wsparcia ze strony rodziny za pośrednictwem dostępnych metod wykorzystujących nowoczesne techniki komunikacji: internet, telefon, wideokomuniacja. Poza tym rodząca kobieta z COVID-19 ma prawo do wszystkich innych praw wynikających z Rozporządzenia Ministra Zdrowia o Standardzie Opieki Okołoporodowej.
TUTAJ MIAŁY POJAWIĆ SIĘ INFORMACJE DOTYCZĄCE KOBIET RODZĄCYCH Z POTWIERDZENIEM COVID-19, LUB PUI – PODEJRZENIEM (Z KWARANTANNY I PO TZW KONTAKCIE BEZ POTWIERDZENIA) JEDNAK ZE WZGLĘDU NA DUŻE ROZBIEŻNOŚCI POMIĘDZY ZALECANIAMI KONSULTANTÓW KRAJOWYCH W STOSUNKU DO ZALECEŃ WHO I TOWARZYSTW POŁOŻNICZO-GINEKOLOGICZNYCH ORAZ NEONATOLOGICZNYCH INNYCH KRAJÓW POSTANOWIŁAM ZREZYGNOWAĆ Z TEJ CZĘŚCI ARTYKUŁU, BY NIE WPROWADZAĆ NIEPOKOJU W KOBIETACH CIĘŻARNYCH.
JEŚLI POTRZEBUJESZ POMOCY LUB INFORMACJI MOŻESZ SIĘ ZE MNĄ SKONTAKTOWAĆ TELEFONICZNIE. INFORMACJE ZNAJDZIESZ NA STRONIE KONTAKT
INFEKCJA KORONAWIRUSOWA PODCZAS KARMIENIA PIERSIĄ
WHO zaleca kontynuację karmienia piersią – nie stwierdzono obecności wirusa w pokarmie kobiecym, a korzyści wynikające z kontynuacji karmienia piersią takie jak przekazanie dziecku przeciwciał przewyższają, nad ewentualnym ryzykiem wynikającym z zarażenia dziecka SARS-CoV-2. Wymagane jest jednak zachowanie ścisłych zasad higieny oraz ograniczenie kontaktu z dzieckiem.
- zanim dotkniesz dziecka, myj ręce ciepłą wodą i mydłem, przynajmniej przez 30 sekund
- używaj maseczki na twarz
- nie śpij z dzieckiem o okresie infekcji
jeśli odciągasz pokarm pamiętaj o:
- myciu rak przed jego dotknięciem,
- założeniu maseczki
- sterylizowaniu sprzętu przed pozyskiwaniem pokarmu, aby zapewnić jego najwyższą sterylność.
ZALECENIA ŚWIATOWEJ ORGANIZACJI ZDROWIA DLA KOBIET W OKRESIE CIĄŻY PORODU I KARMIENIA PIERSIĄ
DOTACJA
Prowadzenie bloga to koszt, pomagamy i piszemy PRO BONO (nie zarabiamy), a przychodzi termin płatności za serwer i domenę, pozostaje nam prosić Was o wsparcie.
Poniżej znajdują się linki do mikropłatności na kwotę 2, 5, lub 10 PLN.
Każda z was może wybrać, która kwota jej odpowiada, liczy się każda złotówka.
Wszelkie nadwyżki, które się pojawią zostaną przekazane na zakup literatury fachowej lub dostęp do wirtualnych baz artykułów medycznych.
Z góry wam dziękuję
Pozdrawiam
Dotacja PLN 2
Dotacja PLN 5
Dotacja PLN 10
LITERATURA
- Mikrobiologia lekarska. Red. Heczko, Piotr B.; Pietrzyk, Agata; Wróblewska, Marta. Warszawa: PZWL Wydawnictwo Lekarskie, 2014, 824 s
- https://doi.org/10.1016/j.jare.2020.03.005
- https://doi.org/10.1016/j.meegid.2020.104212
- https://www.worldometers.info/coronavirus/coronavirus-incubation-period/
- Andersen, K.G., Rambaut, A., Lipkin, W.I. et al. The proximal origin of SARS-CoV-2. Nat Med (2020). https://doi.org/10.1038/s41591-020-0820-9
- uo, Y., Cao, Q., Hong, Z. et al. The origin, transmission and clinical therapies on coronavirus disease 2019 (COVID-19) outbreak – an update on the status. Military Med Res 7, 11 (2020). https://doi.org/10.1186/s40779-020-00240-0
- https://www.cdc.gov/coronavirus/2019-ncov/prepare/pregnancy-breastfeeding.html